8.1.5.Физиология микроорганизмов
8.1.5.Физиология микроорганизмов
Физиология изучает процессы, происходящие в организме. Бактериальная клетка вырабатывает и выделяет в окружающую среду экзоферменты, которые переводят питательные вещества в состояние истинных растворов. Эти растворы под влиянием осмоса проходят через внешнюю оболочку клетки, при помощи другой группы ферментов (эндоферментов) переводятся в состояние коллоидов и свободно проходят через внутреннюю оболочку. С участием соответствующих эндоферментов коллоиды разрушаются, а потом синтезируются в биомассу. Часть питательных веществ расходуется для энергетических нужд, а остальная затрачивается на рост клеток. Образующиеся продукты метаболизма (жизнедеятельности) переводятся в растворимое состояние и выводятся из клетки. Между клеткой и водной средой происходит массобмен, заключающийся в поступлении питательных веществ, и в удалении продуктов метаболизма. Массобмен лимитируется условиями диффузии молекул субстрата и продуктов метаболизма через слой связанных с клеткой молекул воды (слой Нернста). Его толщина зависит от гидродинамических условий и максимальна, если скорость относительного движения клеток и потока воды близка к нулю. Таким образом, в неподвижной воде условия массобмена неблагоприятны, что понижает физиологическую активность клеток (8.7).
В зависимости от рода питания различают метатрофы, использующие органику, и прототрофы, использующие неорганические соединения.
Эндогенным дыханием микроорганизмов называется процесс получения энергии, необходимой для жизнедеятельности. Этот процесс осуществляется путем ферментивных окислительно-восстановительных реакций.
В них участвуют ферменты из группы оксиредуктаз. Механизм процесса заключается в переносе электронов от субстрата к акцептору, которым может быть кислород или молекулы с ненасыщенными связями. Отрыв электронов происходит при окислении атомов водорода, входящих в состав вещества субстрата, до Н+, а также азота, серы и других доноров (табл. 8.3).
Если акцепторами электронов является несвязанный кислород – дыхание называется аэробным, в других случаях – анаэробным.
Микроорганизмы, ферменты которых участвуют в процессах дыхания, относятся, соответственно, к аэробным и анаэробным.
При аэробном дыхании выход энергии в несколько раз выше, чем при аеаэробном. Поэтому анаэробные процессы сравнительно с аэробными замедленны, а количество энаэробов, необходимых для минерализации единицы массы органики, значительно больше, чем аэробов.
Таблица 8.3
Характеристика некоторых процессов эндогенного дыхания
|
Донор электронов |
Акцептор электронов |
Продукт реакции |
Микро- организмы |
|
H |
O2 |
H2O |
Водородные бактерии |
|
H |
SO42– |
H2O; S2– |
Desulfovibrio |
|
Органические вещества |
O2 |
CO2; H2O |
Многие бактерии |
|
NH3 |
O2 |
NO2–; H2O |
Нитрифицирующие бактерии |
|
NO2– |
O2 |
NO3–; H2O |
–––//–––– |
|
Fe2+ |
O2 |
Fe3+ |
Железобактерии |
|
S2– |
O2 |
SO42–; H2O |
Сульфобактерии |
Для жизнедеятельности клеток необходимы основные элементы питания (углерод, азот, кислород, водород и фосфор), а так же микроэлементы: железо, марганец, сера, калий и другие. Если содержание необходимых элементов недостаточно, их следует дополнительно вносить в воду, направляемую на биохимическую очистку (биогенные добавки).
8.1.6. Закономерности синтеза биомассы
В процессе развития микробиальной культуры происходит прирост ее массы. Скорость прироста зависит от многих факторов: обеспеченности питательными веществами, соотношения компонентов, входящих в состав субстрата, накопления в воде продуктов метаболизма или других ингибиторов. Факторы, радикально влияющие на прирост биомассы, называются лимитирующими.
Скорость прироста биомассы может оцениваться по своему абсолютному значению и в каждый момент времени равна:
Vnp = dm / dt,
где dm – прирост биомассы за период времени dt.
Чаще в расчетах используется понятие об удельной скорости прироста М, равной абсолютной скорости, отнесенной к исходной массе m.
Если процесс идет только в присутствии одного лимитирующего компонента, то удельная скорость прироста биомассы прямо пропорциональна его конечной концентрации S*:
M = k [S*].
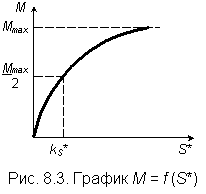 |
Константа скорости реакции k есть ее скорость при условии, что концентрация S* постоянна и равна единице. На рис. 8.3 приведен график, устанавливающий связь между удельной скоростью М и концентрацией лимитирующего компонента [S*]. Форма графика аналогична графику на рис. 8.2. Величина удельной скорости прироста определяется по формуле Моно:
|
где М – удельная скорость роста, Мmax – максимальная удельная скорость роста, [S*] – остаточная концентрация лимитирующего вещества, KS* – константа реакции, численно равная концентрации лимитирующего вещества для скорости прироста, равной половине максимальной. При избытке лимитирующего вещества (если оно необходимо для роста) устанавливается постоянная и максимальная удельная скорость, а KS* = 0.
Если лимитирующим является вещество, угнетающее культуру, например, продукты метаболизма, то удельная скорость М*:
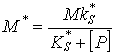 , (8.6)
, (8.6)
где М – удельная скорость прироста в случае отсутствия угнетающего вещества, [Р] – концентрация угнетающего вещества.
Уравнение Моно чрезвычайно упрощено, что следует учитывать при его применении.
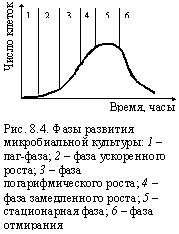 |
Принципиальные закономерности развития микробиальных культур можно проследить по результатам наблюдений за их ростом в неподвижной среде. Развитие культуры проходит несколько фаз (рис. 8.4). Первоначально (первая фаза) происходит адаптация, увеличивается размер клеток и это приводит к некоторому приросту биомассы. Затем (вторая и третья фазы), абсолютная скорость роста увеличивается, а относительная остается постоянной. Фаза замедленного роста характеризуется уменьшением относительной и абсолютной скоростей, а прирост биомассы менее интенсивен. Для пятой, стационарной фазы рост и отмирание клеток приближаются к равновесию; наконец, наступает фаза отмирания и происходит автолиз клеток (автолиз – отмирание и распад клеток под действием ферментов, выделяемых живыми клетками).Удельная скорость роста зависит от физиологической активности клетки qф. Физиологическая активность характеризует потребность клетки в питательных веществах для обеспечения нормальных условий жизнедеятельности и при их ухудшении снижается. Физиологическая активность определяется по зависимости: |
qф = аМ + в, (8.7)
где а – трофический коэффициент, показывающий затраты питательных веществ на образование единицы биомассы, в – коэффициент основного обмена, показывающий расход питательных веществ на поддержание жизни единицы биомассы в течение одного часа.
Коэффициенты а и в для определенной культуры и стабильных условий ее развития есть величины постоянные.
В процессе биохимической очистки прирост биомассы должен быть минимальным, т.к. при этом упрощается иловое хозяйство. Снижение скорости роста приводит к более глубокому распаду субстрата, но связано с уменьшением физиологической активности микроорганизмов. Как следует из рис. 8.4 оптимальные для очистки условия складываются в пятой, стационарной фазе развития. В тех случаях, когда глубокая очистка не требуется, возможен процесс очистки и для условий третьей фазы (логарифмического роста), а при необходимости максимально глубокой очистки – процесс ведется в условиях фазы отмирания.
8.1.7. Влияние внешних факторов на микроорганизмы
К основным внешним факторам относятся: температура воды, ее химический состав, концентрация субстрата.
Влияние температур. Температура воды влияет на скорость ферментивных реакций и на структуру клеточных компонентов. В соответствии с этим результат изменения температуры проявляется немедленно или, а в последнем случае, после достаточно длительного температурного воздействия.
По отношению к температуре, требующейся для нормальной жизнедеятельности, микроорганизмы делятся на три группы: психрофилы, мезофилы и термофилы.
Психрофилы (психрос – холод) приспособлены к существованию при температурах от –8 до +10 °С, но жизнеспособны и при более высоких температурах (до +30 °С). Физиологическая активность психрофилов мала и их редко используют в системах очистки.
Мезофилы (мезо – средний) нормально развиваются в интервале температур от +15 до +40 °С, хотя этот интервал условен. Биохимическая очистка воды обычно производится культурами мезофильных микроорганизмов.
Термофилы (термо – тепло) жизнеспособны при температурах от 30 до 70 °С. Как и в других случаях интервал температур условен и для разных культур различен.
Для конкретных культур существуют оптимальные значения температур. Так, для термофильных микроорганизмов, при помощи которых происходит анаэробная стабилизация осадков, оптимальной считается температура +52 – 53 °С, для мезофильных при аэробной очистке сточных вод в биофильтрах и аэротенках допустимы температуры до +25 °С и т.д.
Постепенное изменение температур воды в относительно больших интервалах не опасно для микроорганизмов, которые способны адаптироваться к новым условиям. Вместе с тем, внезапное изменение температуры воды даже в пределах 10–15 °С способно вызывать массовое отмирание микроорганизмов.
Влияние химического состава. Значение рН влияет на состояние ферментов и, в частности, на структуру белковой части их молекул.
Оптимальные значения рН различны для разных ферментов и ограничены интервалом 1–2 единицы, хотя область, в которой соответствующие микроорганизмы могут существовать, достигает 5–6 единиц.
В зависимости от рН биохимические процессы могут идти по разным маршрутам с получением разных конечных продуктов. Так, если денитрификация осуществляется при рН более 7, конечный продукт – молекулярный азот, если рН менее 7, то NO или N2O.
Аэробные процессы носят окислительный характер и для них значение окислительно-восстановительной мощности системы rН2 должна составлять не менее 20 – 25. Как следует из рис. 6.14 значение Еn следует поддерживать в пределах +0,2 – +0,4 В. Повышение rН2 до 30 и более нежелательно, т.к. избыток кислорода угнетающе действует на микроорганизмы. В процессе аэробной очистки rН2 уменьшается.
Для анаэробных процессов окислительно-восстановительная мощность системы принимается около 10–12, но не более 18–20. Последнее условие связано с ограничением насыщения кислородом воды при анаэробной очистке.
В ходе анаэробной очистки rН2 несколько увеличивается.
Химические вещества могут оказывать на популяцию микроорганизмов как угнетающее, так и стимулирующее влияние. Это зависит от дозы примеси, от присутствия других примесей, взаимодействующих с данной, продолжительности контакта, рН, Е, температуры воды и других.
Так, при концентрации аммиака до 250 мг/л анаэробный процесс в метантенках интенсифицируется, при 250–1200 мг/л определенное воздействие не проявляется, 1800–3500 мг/л – возникает ингибирование процесса, а при больших концентрациях аммиак токсичен по отношению к клеткам.
Наибольшее бактерицидное влияние фенолов проявляется при концентрации 50 мг/л, этилового спирта – 70 мг/л и т.д. ПДК веществ в воде, поступающей на биохимическую очистку, обычно принимается 15–30 % от концентраций, обуславливающих максимальное токсическое воздействие. Так, ПДК фенолов составляет 15 мг/л, этилового спирта – 14 мг/л. ПДК свинца, кадмия, титана, шестивалентного хрома – 0,1 мг/л, а ртути – 0,001 мг/л.
Одновременное присутствие нескольких разных примесей может либо взаимно усилить ингибирование, т.е. торможение путем понижения активности ферментов (эффект синергизма), либо, наоборот, снизить угнетающее влияние (антогонизм).
Микробы адаптируются к различным химическим веществам при условии, что концентрации последних меняются постепенно. Продолжительность адаптации зависит от конкретных условий и продолжается от 1–2 суток до нескольких месяцев [28].
Процесс адаптации приводит к увеличению сродства вырабатываемых клетками ферментов с субстратом, либо к изменению скорости продуцирования фермента.
В первом случае меняется состав биоценоза, во втором – состав остается прежним, но изменяется активность клеток.
Адаптация, которая сопровождается перестройкой биоценоза и накоплением адаптированных форм микроорганизмов, необходима при очистке промышленных сточных вод, содержащих такие примеси, как бензол, толуол, метилфениловый эфир, некоторые альдегиды (фурфурол, акролеин, бензойный и масляный альдегид), хлорфенол, многие нитрилы и СПАВ.
Влияние концентрации субстрата. Изменение концентрации субстрата требует адаптации микробов чаще всего путем изменения микробиальной массы, в результате чего восстанавливается равновесие между содержанием субстрата и количеством вырабатываемого фермента.
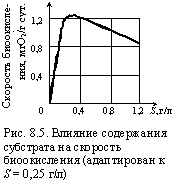 |
Для установки биохимической очистки (например, для аэротенка), работающей в стационарных условиях, микробиальная масса (активный ил) находится в адаптированных условиях. Если концентрация субстрата не превышает уровня, при котором произошла адаптация, то скорость изъятия загрязнений обусловлена содержанием субстрата. Повышение его концентрации сверх оптимального не приводит к увеличению скорости изъятия, а наоборот, понижает ее (рис. 8.5). Оценивая влияние концентрации субстрата на скорость биохимической очистки констатируем, что между концентрациями субстрата и ферментов существует прямая зависимость. В стабильных условиях эти концентрации оказываются сбалансированными. |
При нарушении баланса путем повышения концентрации субстрата сравнительно со сложившимся адаптационным уровнем, скорость процесса лимитируется концентрацией фермента, отвечающей адаптационному уровню. Если концентрация субстрата понизится сравнительно с адаптационной, то скорость процесса будет зависеть только от концентрации субстрата.
Мутация (от лат. – изменение) части клеток меняет биохимические условия и характер ферментов, вырабатываемых бактериальной массой. Нередко это приводит к позитивным результатам: интенсификации процесса деструкции субстрата или к расширению диапозона соединений, подвергающихся биохимической очистке.
Специальная обработка биомассы с целью вызвать мутацию клеток (мутагенез) осуществляется как химическими (с использованием реагентов), так и физическими методами (ультразвуковое облучение, магнитная обработка, создание электрического поля, гидродинамическая обработка). Мутагенез проводится для 0,1 % и менее от общего количества клеток биомассы.
По исследованию НИИ ВОДГЕО гидродинамический мутагенез активного ила аэротенков для очистки городских сточных вод, разрушающий защитный слой Нерста, повышает производительность сооружения на 150–250 %, снижает иловый индекс на 30–50 %, прирост избыточного ила – на 30–80 % [34].
8.2. Биохимические процессы очистки в аэробных условиях
8.2.1. Общие сведения
Биохимическая очистка от органических соединений осуществляется с участием гетеротрофов, т.е. микроорганизмов, для которых источником питания является углерод органики: белков, жиров, углеводов, углеводородов и т.д. Ц.И. Роговская отмечала, что питательная ценность источников углерода различна и зависит как от их физико-химических свойств, так и от физиологических особенностей микроорганизмов. В процессе жизнедеятельности микробов часть атомов углерода окисляется сперва до СО или СООН, а затем до углекислого газа. Часть атомов углерода восстанавливается до радикалов СН3 – СН2 = СН и входят в состав клетки [28].
Биохимическое разрушение органики происходит в результате ряда последовательных реакций, при которых первоначальная структура вещества постепенно упрощается.
8.2.2. Биохимическая деструкция белков
Белки состоят из молекул аминокислот, в состав которых входят карбоксильные (СООН) и аминогруппы (NH2–), соединенные атомом углерода, а также углеродный радикал R
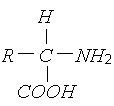 .
.
Эти группы формируют длинноцепочные молекулы с большой молекулярной массой.
Белки непосредственно не усваиваются микробами, но под действием экзоферментов гидролизуются с образованием соединений с меньшей молекулярной массой.
Аминокислоты различаются строением радикалов, которые могут быть углеводородными соединениями (СН3 и других), но иногда включают группы ОН, NH3, СООН, ароматическое ядро. Разнообразие белковых молекул обусловлено вариантами последовательности соединения аминокислот.
Под действием экзоферментов цепочки аминокислот расщепляются и этим переводятся в состояние, удобное для поглощения клетками. В результате внутриклеточных процессов с участием эндоферментов аминокислоты окисляются с выделением свободного аммиака (процесс аммонификации):
RCHNH2COOH + 0,5O2 ![]() RCOCOOH + NH3.
RCOCOOH + NH3.
Аммонификация может проходить и по другим схемам путем восстановления:
RCHNH2COOH + 2H = RCH2COOH + NH3,
и прямым путем (деструкцией):
RCHNH2COOH → RCHCHCOOH + NH3.
Помимо аммиака продуктом распада являются кетокислоты, взаимодействие которых с аминокислотами приводит к образованию менее устойчивых кислот (процесс переаминирования):
R1CHNH2COOH + R2COCOOH→ R1COCOOH + R2CHCNН2COOH.
В состав некоторых белков входит сера, которая при гидролизе восстанавливается до сероводорода.
Под действием серобактерий сероводород окисляется до серы, накапливающейся в клетках, на на втором этапе под влиянием эндоферментов образуются сульфаты:
2H2S + O2 = 2S + 2H2O,
2S + O2 + 2H2O = 2H2SO4.


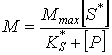 , (8.5)
, (8.5)

