8.2.3. Биохимическая деструкция жиров
8.2.3. Биохимическая деструкция жиров
Жиры состоят из молекул глицеридов, сложных эфиров глицерина и высших кислот. Общая формула глицеридов имеет вид:
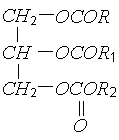
где R, R1, R2 – углеводородные радикалы.
Жиры легко гидролизуются с участием экзофермента липазы и разделяются на глицерин и соответствующую жирную кислоту:
С3Н5(С18Н35О2)3 + 3Н2О ![]() С3Н5(ОН)3 + 3С18Н36О2.
С3Н5(ОН)3 + 3С18Н36О2.
глицерин стеариновая кислота
В ходе внутриклеточных процессов глицерин окисляется до углекислого газа и воды. Жирные кислоты с трудом поддаются окислению и этот процесс включает ряд этапов. На каждом из них жирная кислота теряет по две метильные группы СН2 и постепенно расщепляется до углекислого газа и воды.
8.2.4. Биохимическая деструкция углеводов
Углеводами (сахарами) называются органические соединения, для большинства которых справедлива общая формула (СН2О)n, где n ≥ 3. В биосфере вещества углеводной природы (включая крахмал и целлюлозу) превосходят по массе другие органические соединения, вместе взятые.
Биохимическая деструкция углеводов с получением в качестве конечного продукта углекислого газа и воды – многоступенчатый процесс. Рассмотрим это на примере деструкции глюкозы. На первом этапе в анаэробных условиях образуется пировиноградная кислота СН2СОСООН и выделяется углекислый газ. Последующая деструкция проходит в аэробных условиях с участием нескольких групп бактерий по круговому циклу (цикл Кребса). При этом последовательно образуются трехкарбоновые кислоты (лимонная, цисаконтелитовая и другие) вплоть до щавелевоуксусной. При этом на отдельных этапах выделяется и удаляется СО2. Конечный продукт кругового цикла – щавелевоуксусная кислота, соединяясь с углекислым газом, образует вновь пировиноградную кислоту. Однако, вследствие общих потерь СО2 в цикле, количество этой кислоты и исходного продукта (глюкозы) уменьшается.
Аналогично разрушаются и другие полисахара, но они, в отличие от глюкозы расщепляются специализированными группами микробов (глюкозу хорошо усваивают многие виды микроорганизмов). Цикл Кребса может оставаться незавершенным; тогда в воде остаются промежуточные продукты – различные трехкарбоновые кислоты.
Целлюлоза (клетчатка) разрушается специализированными миксобактериями при их непосредственном контакте с целлюлозой. Грибы родов Fusarium, Truchoderma и других гидролизуют целлюлозу по обычной схеме – путем выделения во внешнюю среду экзоферментов. После гидролиза процесс дальнейшего расщепления осуществляется внутри клетки с помощью эндоферментов.
8.2.5. Биохимическая деструкция нуклеиновой кислоты
Нуклеиновая кислота, – биологически активный биополимер, входящий в состав клеток всех организмов. Под действием многих бактерий (Nacordia, Micobacterium и др.). Молекулы нуклеиновой кислоты разрушаются с образованием мочевой кислоты, при гидролизе которой образуется мочевина CO(NH2)2, а также тартоновая кислота:
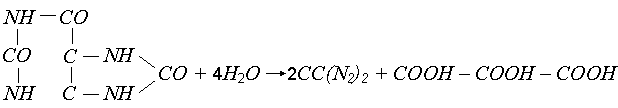 .
.
Мочевина, в свою очередь, гидролизуется с участием фермента уразы:
CO(NH2)2 + H2O ![]() CO2 + 2NH3.
CO2 + 2NH3.
Нитрифицирующие микроорганизмы окисляют мочевину, мочевую кислоту и аммиак, причем органическую часть молекул органики нитрификаторы не используют, а необходимую для жизнедеятельности энергию получают путем окисления солей аммония, являющихся донорами электронов. Как и в других аэробных процессах их акцептором является кислород. Нитрифицирующие микробы угнетаются аэробами-гетеротрофами и активизируются только после того, как запасы питательных веществ в воде истощаются, развитие гетеротрофов замедляется, в воде накапливается NH3 и О2. Клетки нитрификаторов генерируются очень вяло.
Аммонийные соли преобразуются двумя группами нитрифицирующих бактерий в нитриты, а затем в нитраты:
2NH3 + 3O2 = 2HNO2 + H2O,
2HNO2 + O2 = 2HNO3.
Этот процесс нитрификации происходит с выделением тепла при оптимальных температурах от 20 до 35 °С, проходит с постоянной ограниченной скоростью при температурах 9–20 °С и прекращается при температуре около 0 °С.
В соответствии со стехиометрическими расчетами на окисление 1 г аммонийного азота расходуется в г О2: в нитриты – 3,43 г; а в нитраты – 4,57 г.
В состав нуклеиновой кислоты (а так же некоторых других органических соединений) входит фосфор, который в процессе деструкции органики освобождается в виде фосфорной кислоты, образующей трудно растворимые фосфаты, например, Са(НРО4)2.
При взаимодействии с кислотами происходит расторжение этих соединений с образованием Са(НРО4)2 и других.
8.2.6. Биохимическая деструкция углеводородов
Углеводороды (к ним помимо рассмотренного выше углеводов) относятся различные виды нефти, угля, горючих газов и продуктов их переработки. Углеводороды – характерный вид загрязнений, присутствующий в промышленных сточных водах. Как и в рассмотренных случаях биохимическая деструкция углеводородов – многостадийный процесс, сопровождающийся образованием ряда промежуточных продуктов (органических кислот и спиртов). Разрушение углеводородов чаще всего осуществляется адаптированными микроорганизмами. Конечными продуктами при полной деструкции являются СО2 и Н2О. Изучение условий биохимической деструкции углеводородов позволило определить только несколько частных случаев, когда выявляется закономерность этого процесса и имеется возможность его четкого прогнозирования.
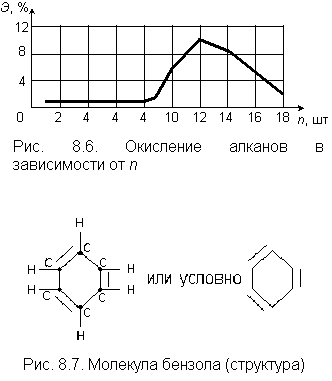 |
Алканы (предельные углеводороды) имеют обобщенную формулу СnH2(n+1), где n = 1–20. При n ≤ 4 алканы – газообразные вещества (метан и другие), при 5–15 – жидкие (пентан–декан), при 16 и 20 – твердые (пентадекан и эйкозан). Алканы являются составной частью нефти и присутствуют в стоках, загрязненных нефтепродуктами. Установлено, что при n ≤ 5 алканы не окисляются, при 6–8 они токсичны, при 9–14 – окисляются незначительно. В наибольшей степени поддается биохимическому окислению додекан СН3(СН2)10СН31 (рис. 8.6). Биохимическое окисление алканов может происходить по нескольким маршрутам: «предельные углеводороды – непредельные углеводороды – спирты – кетоны – жирные кислоты – конечные продукты (углекислый газ и вода)»; «алканы – кетоны – первичные жирные кислоты – конечный продукт». В зависимости от условий прохождения процесс может остановиться на одном из промежуточных этапов. Ароматические углеводороды или арены имеют обобщающую формулу СnH2n–6. Например, для бензола n = 6, для толуола n = 7 и т.д. Молекулы ароматических углеводородов включают бензольное кольцо, обладающее повышенной устойчивостью. Устойчивость кольца обусловлена его симметричностью с чередованием простых и двойных связей между атомами углерода. На рис. 8.7 приведена структурная схема молекулы бензола. |
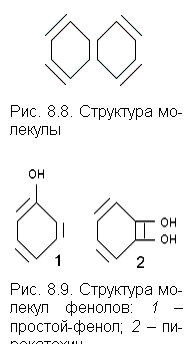 |
Менее устойчивыми оказываются полициклические ароматические углеводороды, состоящие из нескольких бензольных колец (рис. 8.8). Начальным этапом деструкции ароматических соединений является присоединение к кольцу гидроксил–ионов, т.е. гидроксилирование. При этом образуются производные соединения: фенолы, обладающие большей реакционной способностью, чем исходные продукты. Так, при присоединении одной группы ОН– молекула бензола превращается в простой фенол, двух – в пирокатехин и т.д. (рис. 8.9). Дальнейшая деструкция связана с разрывом бензольного кольца. Разрыв может возникнуть в месте двойной связи между двумя соседними гидроксилированными атомами углерода, между одним гидроксилированным и соседним негидроксилированным атомом углерода, между углеродными атомами, несущими боковую цепь. Аналогично происходит деструкция и полициклических углеводородов. |
8.2.7. Биохимическая деструкция загрязнений бытовых сточных вод
В бытовых сточных водах органические загрязнения состоят в основном из углерода, азота, кислорода и водорода; гипотетический состав примесей выражается формулой: CxHyOzN. В бытовых стоках в достаточных концентрациях содержатся фосфор и другие биогенные элементы, необходимые для жизнедеятельности микроорганизмов (табл. 8.4).
Таблица 8.4
Важнейшие источники образования химических элементов
при биохимической деструкции
|
Источник |
Элемент |
|
СО2, сахара, белки, жиры |
Углерод |
|
Белки, NO2–, NO3– |
Азот |
|
Сера, белки, SO42– |
Сера |
|
РО43– |
Фосфор |
Минерализация органики в аэробных условиях протекает в два этапа: на первом под влиянием экзоферментов и с участием кислорода часть органических веществ окисляется до аммиака, воды и углекислого газа, на втором с участием аммиака и кислорода в результате ферментивной реакции происходит разрушение остальной органики, синтез биомассы микроорганизмов, образуется вода и углекислый газ. Затраты кислорода на эти два вида реакции в сумме равны БПКп исходной воды.
Прирост биологической массы в результате ее синтеза может быть оценен в зависимости от того, какая доля электронов в ходе окислительно-восстановительного процесса затрачивается в реакциях синтеза и выработки энергии, т.е. от физиологической активности клеток.
8.2.8. Аэробное окисление железа и марганца
Двухвалентное железо и двухвалентный марганец окисляются до малорастворимого состояния хемисинтезирующими аэробными микроорганизмами. Такие микроорганизмы ассимилизируют углекислоту, используя для этого электроны, выделяющиеся при реакции окисления.
К железобактериям относится большая группа микроорганизмов, окисляющих двухвалентное железо в трехвалентное:
4Fe(HCO3)2 + 6H2O+O2 = 4Fe(OH)3 + 4H2CO3 + 4CO2.
Окисление двухвалентного марганца может осуществляться многими микроорганизмами и проходит согласно реакции:
Mn2+ + ½ O2 + 2OH– = MnO2 + H2O.
Продукт окисления пиролюзит (двуокись марганца) является катализатором различных реакций окисления.
Выход энергии при окислении марганца мал и недостаточен для энергообеспечения марганцеокисляющих микробов. В работе [19] делается вывод, что «превращение марганца не относится к жизненоважным функциям организмов, а является побочной реакцией».
Микробиальные методы обезжелезивания (деферизации) и деманганации реализованы в схеме очистки подземных вод в пласте (способ «Веридекс»). Этот способ, как отмечает профессор Г.И. Николадзе, эффективен при достаточно высоких значениях рН и в присутствии кислорода [29]. Необходимое значение рН оределяется в зависимости от окислительно-восстановительного потенциала Е устойчивую деманганацию следует ожидать при мощности редокссистемы rH2 > 34 – 35 (рис. 6.14).
Деферизация и деманганация достигаются при пропуске воды через двухступенчатые биофильтры, первая ступень которых обеспечивает главным образом, биохимическое удаление железа, а вторая – марганца.
Для деманганации применяют зернистые фильтры, на поверхности зерен загрузки производится высев марганцеокисляющих микроорганизмов [30].
8.3. Биохимические процессы очистки в анаэробных условиях
8.3.1. Общие сведения
Как отмечалось, принципиальным отличием анаэробных процессов от аэробных является то, что анаэробные микроорганизмы используют в качестве акцептора электронов некоторые органические или неорганические соединения, содержащие связанный кислород. Соответствующие ферментивные реакции, называются бродильными. Хотя брожение и вызывает расщепление органики, но не обеспечивает ее полный распад.
Следует отметить, что энергетический эффект, достигаемый при анаэробном процессе, на порядок ниже, чем при аэробном. В [31] приводится следующий пример. При аэробном окислении одной молекулы виноградного сахара выделяется в 25 раз больше энергии, чем при анаэробном. Поскольку потребность в энергии бактериальной клетки одинакова, независимо от того, является ли она аэробной или анаэробной, анаэробам приходится перерабатывать значительно больше вещества для обеспечения своих энергетических нужд, чем аэробам. Поэтому распад органики в ходе анаэробных процессов неполный и протекает замедленно.
Анаэробная очистка от органики осуществляется в результате одного из видов брожения – метанового, при котором основная часть загрязнений газифицируется с образованием метана.
Метановое брожение включает два этапа. На первом протекают процессы гидролиза и ферментивные реакции расщепления белков, углеводов и жиров с образованием органических кислот жирного ряда. Кроме того, продуктами распада являются спирты, углекислота, аммиак, водород и другие. Главный продукт первого этапа брожения – уксусная кислота (70 %). На втором этапе под воздействием метанообразующих бактерий происходит распад уксусной кислоты и, параллельно, восстановление водородом углекислого газа согласно уравнениям:
СН3СООН ![]() СН4 + СО2,
СН4 + СО2,
СО2 + 8Н ![]() СН4 + 2Н2О.
СН4 + 2Н2О.
Таким образом, в качестве конечных акцепторов электронов используется связанный кислород.
Анаэробная деструкция часто неэффективна. Так, в анаэробных условиях не разрушаются углеводороды, целлюлоза; глубина анаэробного распада органики малоконцентрированных бытовых сточных вод в пересчете на беззольное вещество не превышает 50–55 %.
Однако в ряде случаев возможны только анаэробные методы биологической очистки: денитртфикация, дефосфатирование и другие.
Важной особенностью анаэробного процесса является крайне малый (на порядок меньше, чем в аэробных процессах) прирост микробиальной массы. Поэтому при биологической очистке высококонцентрированных стоков, содержащих органические загрязнения и имеющих БПКполн более 1–2 г/л и до 20 г/л, на первом этапе применяется анаэробная очистка, обеспечивающая снижение БПК на 90 %.
Следует отметить особую чувствительность метанообразующих микроорганизмов к физико-химическим условиям. В наибольшей степени это относится к термофильным микроорганизмам.
8.3.2. Анаэробная денитрификация
В анаэробных условиях происходит денитрификация – восстановление нитритов и нитратов.
Денитрификаторы относятся к категории факультативных микроорганизмов, т.е. в зависимости от конкретных условий они ведут себя как аэробы или как анаэробы. Денитрификация происходит при дефиците кислорода в воде, т. е. в условиях неблагоприятных для конкурирующих гетеротрофных аэробов. Дентирификаторы используют в качестве акцептора электронов связанный кислород, входящий в состав нитритов и нитратов, передавая ему электроны окисляемой органики (углеводов, аминокислот, органических кислот и других). При недостатке органики в воду следует добавлять углеродосодержащие примеси, например, метиловый спирт. Общая схема денитрификации, включая ряд промежуточных продуктов, имеет вид:
NO3– → NO2 → NO → N2O → N2↑.
Процесс денитрификации, во время которого микроорганизмы окисляют органическое вещество (СН3ОН), используя связанный кислород, входящий в состав нитратов, может быть записан в следующем виде:
![]() .
.
Таким образом, рН воды, понизившийся при нейтрализации, вновь повышается.
Денитрификация проходит при дефиците кислорода, т.к. использование свободного кислорода как акцептора электронов дает больший выход энергии, чем связанного. Процесс нуждается в присутствии органики. Значение 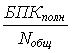 должно быть не менее 3,5–4,0.
должно быть не менее 3,5–4,0.
В процессе денитрификации происходит выделение кислорода: при восстановлении нитратов в нитриты – 1,71 г, нитритов в азот –2,85 г кислорода в расчете на 1 г азота. Полная денитрификация происходит при рН = 7,0.
8.3.3. Анаэробное восстановление тяжелых металлов
В этих процессах соединения металлов являются только источниками связанного кислорода, как акцептора электронов. Соответствующие анаэробы по характеру питания относятся к гетеротрофам, т.е. имеющим смешанное питание и нуждающихся в готовых органических соединениях.
Чаще всего восстановление металлов может осуществляться различными анаэробами, т.е. не иметь специфических возбудителей. Среди восстанавливаемых металлов молибден, теллур, селен, ртуть. Достаточно хорошо исследовано биохимическое восстановление шестивалентного хрома в трехвалентный [32].
Процесс протекает активно при минимальной затрате субстрата, который, окисляясь, служит донором электронов: этилацетата, пропилового и изопропилового спирта, отработанного трансформаторного масла и других углеродосодержащих веществ.
8.4. Сооружения для аэробной очистки сточных вод
8.4.1. Общие сведения
Городские и промышленные сточные воды представляют собой многокомпонентные по составу и дисперсности частиц смеси. Клеточная масса, используемая для очистки, включает значительное количество различных культур, находящихся в неоднозначных взаимоотношениях. Часто продукты жизнедеятельности одних культур служат источником питания других. Возможны ситуации, при которых между отдельными культурами возникает антагонизм и культура, находящаяся в подавленном состоянии, начинает развиваться только тогда, когда условия жизнедеятельности доминировавшей культуры почему либо становятся неблагоприятными. Например, неблагоприятные изменения физико-химического качества воды приводят к бурному развитию сине-зеленых водорослей, что вызывает вспухание активного ила.
Как правило, поступление сточной воды на очистку непрерывное и сооружения работают по проточному режиму. Это может привести в ряде случаев к выносу биологической массы и уносу ферментов.
Биологическая очистка сточных вод целесообразна, если основная масса загрязнений поддается биохимической деструкции и БПК составляет значительную долю от ХПК (табл. 8.2). В зависимости от типов очистных сооружений БПКп сточной воды может быть понижено до 15–3 мг/л.
8.4.2. Характеристика биологической массы
В очистных сооружениях биологическая масса находится в виде свободно плавающего активного ила или в иммобилизованном (закрепленном) состоянии. Микробиальный состав массы и в том, и в другом случае практически одинаков, а биоценоз включает организмы первых трех трофических уровней.
Активный ил состоит из комочков размерами до 150 мкм, образующих хлопья, взвешенные в потоке сточной воды. Приблизительно 60 % ила представлена культурами микроорганизмов; около 40 % по массе состоит из частиц субстрата, сорбированного илом.
В потоке, оказывающем механическое воздействие на микробиальные клетки, усиливается выделение последними биологических флокулирующих веществ и образование скоплений в виде слизистых капсул (зоогелей). Считают, что вещества, входящие в состав слизи, влияют на электрические заряды клеток, в результате чего клетки находятся на некотором расстоянии друг от друга, хотя и связаны между собой флокулирующими веществами. Такая структура хлопьев делает их прекрасными сорбентами: поверхность хлопьев (в пересчете на сухое вещество) составляет около 1000 м2 на 1 г, т.е. того же порядка, что и активированных углей.
В одном кубическом метре ила содержится до 1014 живых клеток, в том числе 1 % анаэробов.
Биологическая пленка образуется на поверхностях каркасов – носителей в результате иммобилизации (от латинского – неподвижный). Наряду с микробиальной массой в состав пленок входят грибы, плесени, инфузории, личинки насекомых, черви. При увеличении толщины пленки нарушается кислородоснабжение «погребенных» участков, где и возникают анаэробные условия. До 25–28 % микробиальной массы пленки составляют анаэробы. Количество живых клеток на 1 м3 пленки на два порядка меньше, чем в активном иле.
Иммобилизация клеток имеет ряд преимуществ. Активная часть закрепленной биомассы сконцентрирована в поверхностном слое толщиной от 40 до 1000 мкм. Относительная скорость воды у этой поверхности больше, чем у поверхности свободноплавающих клеток. По мнению профессора Н.И. Куликова [33] повышение относительной скорости приводит к уменьшению толщины гидратного слоя Нернста и к увеличению активности клеток. Результатом является уменьшение значения коэффициента Михаэлиса и возрастание скорости ферментивной реакции.
Сочетание аэробных и анаэробных микроорганизмов, входящих в состав пленки, а так же ее сорбционные свойства оказывают позитивное влияние на процесс очистки.
Закрепление биомассы позволяет сформировать ступени очистки с различающимся биоценозом.




