Применение перекиси водорода для окисления железа подземных вод
Окисление железа является одним из ключевых процессов технологии кондиционирования подземных вод при подготовке к фильтрованию через зернистый слой.
Необходимость обезжелезивания подземных вод при их использовании для хозяйственно-питьевого водоснабжения определяется, в первую очередь, негативным влиянием соединений железа на организм человека. Избыток железа оказывает токсическое действие на печень, селезенку, головной мозг, усиливает воспалительные процессы в организме, приводит к дефициту некоторых микроэлементов (медь, цинк и др.).
Требования по извлечению железа из используемой воды вызваны не только гигиеническими соображениями, а целым рядом нежелательных последствий эстетического, технического и экономического характера: следы на белье, посуде и бытовом водопотребляющем оборудовании; коррозия и отложения в трубопроводах; быстрый выход из строя водонагревательных и водоумягчительных систем.
Комплект «ОКСИ-ЛОДЖИКС» для удаления сероводорода и железа
Следует отметить, что разложение перекиси водорода с одновременным окислением йона двухвалентного железа в трехвалентное и ее каталитическое разложение, вызываемое ионами двух- и трехвалентного железа, изучены достаточно подробно. Ион закисного железа окисляется перекисью водорода согласно следующей стехиометрической реакции:
2Fe2+ + Н2O2 + 2 Н+ → 2Fe3+ + 2Н2О. (1)
Эта реакция протекает количественно при избытке иона двухвалентного железа, тогда как при избытке перекиси водорода наряду с окислением закисного железа протекает разложение перекиси водорода с выделением кислорода.
Принято считать, что взаимодействие Н2O2 с аква-ионом Fe2+ приводит к образованию ÓH-радикала в качестве первичной реакционно-способной частицы. Однако образование гидроксил-радикала в этой реакции – лишь частный случай окислительно-восстановительных превращений промежуточного комплекса Fe2+ с Н2O2.
Первичный акт взаимодействия Fe2+ с Н2O2 состоит в замещении координированной молекулы воды:
Н2O2 + Fe2+Н2O ↔ (FeН2O2)2+ + Н2O. (2)
Образование радикалов ÓH в процессе Фентона в кислой среде свидетельствует о том, что в этих условиях образовавшийся пероксо-комплекс распадается преимущественно на продукты одноэлектронного переноса:
(FeН2O2)2+ → Fe3+OH– + ÓH. (3)
Рост скорости окисления двухвалентного железа при рН>3 связан с диссоциацией координированной воды в комплексе, поскольку диссоциация перекиси водорода приводит к уменьшению ее окислительной способности, тогда как диссоциация воды – к существенному снижению окислительно-восстановительного потенциала пары Fe4+/Fe2+, что приводит к облегчению внутрисферного двухэлектронного переноса с последующим образованием гидролизованного феррил-иона:
(FeН2O2)2+ → (OH–)(FeН2O2)2+ + Н+, (4)
(OH–)(FeН2O2)2+→ (OH–)FeО2+ + Н2O. (5)
Эта частица может участвовать либо в окислении воды с образованием ÓH-радикала, либо взаимодействовать со вторым ионом железа без образования свободных радикалов:
(OH–)FeО2+ → Fe3+ (OH–)2 + ÓH, (6)
(OH–)FeО2+ + Fe2+ → 2Fe 3+ OH–. (7)
Вследствие протекания реакций (4,5) с ростом рН эффективная константа скорости окисления Fe2+ перестает зависеть от рН.
Негидролизованный комплекс FeН2O22+, также как и феррил-ион, может взаимодействовать с «третьей» частицей, в частности, со вторым ионом железа также без образования свободных радикалов:
(FeН2O2)2+ + Fe2+ → 2Fe3+ OH–. (8)
Другой тип реакций связан с модификацией промежуточного пероксо-комплекса путем замещения координированной воды на вторую молекулу перекиси водорода. В результате возможно осуществление молекулярного (каталазного) механизма разложения перекиси:
(FeН2O2)2+ + Н2O2 → Н2O2 (FeН2O2)2+ → (НO2FeН2O2)+ → Fe2+ OH– + О2↑ + Н2O. (9)
Установлено, что в нейтральной водной среде увеличение концентрации как ионов Fe2+, так и ионов Fe3+ приводит к росту скорости процесса распада Н2О2, причем этот рост практически не зависит от рН и концентрации перекиси водорода. Установлено также, что спонтанное разложение Н2O2 в этих условиях происходит на микроколлоидных частицах гидроокиси железа и протекает по нерадикальному механизму.
Очевидно, что при использовании перекиси водорода для окисления железа подземных вод возможно протекание всех перечисленных реакций. Процесс значительно усложняется в слабокислых средах, где более вероятно образование ÓH-радикалов, при наличии в воде органических примесей, а также в присутствии примесей доноров водорода, взаимодействующих с феррил-ионом, и при наличии в воде ионов меди, являющихся сокатализаторами процессов распада Н2O2 и окисления органических веществ. Это делает химию процесса обезжелезивания воды с использованием перекиси водорода достаточно сложной.
Тем не менее, такая технология представляет определенный интерес, особенно в тех случаях, когда традиционные методы обезжелезивания оказываются неэффективными. Впервые технология с использованием перекиси водорода испытана применительно к подземным водам севера Тюменской области. Отличительными особенностями состава этих вод являются низкие значения жесткости (0,15÷0,40 мг-экв/дм3), щелочности (0,29÷0,38 мг-экв/дм3) и температуры воды (0,3÷1,40С). Содержание железа общ. составляет 5,5 ÷ 6,2 мг/дм3, в том числе двухвалентного – 4,7÷5,5 мг/дм3. Применение классических методов обезжелезивания для воды такого состава не обеспечивает получения нормативного содержания железа в очищенной воде.
Выполненные лабораторные исследования процесса обезжелезивания подземных вод по схеме «окисление Н2O2 – фильтрование» подтвердили высокую эффективность этого метода.
Работа проводилась в условиях действующего водозабора водопроводных очистных сооружения (ВОС) г. Новый Уренгой в осенне-зимний период, при минимальной температуре обрабатываемой воды.
На первом этапе было изучено окисление двухвалентного железа в свободном объеме. В качестве реакционного сосуда был использован химический стакан емкостью 2 л, установленный на магнитной мешалке. Дозирование перекиси водорода в виде 0,1М раствора производилось при помощи лабораторной пипетки. Отбор пробы воды для определения остаточного железа производился через 1 мин. после внесения реагента.
На рис.1 представлена зависимость остаточного содержания двухвалентного железа в нефильтрованной воде от исходной концентрации перекиси водорода и удельной дозы окислителя.
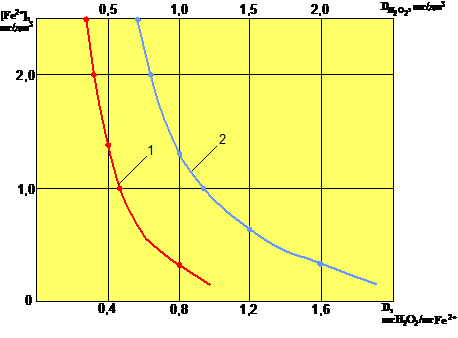
Рис. 1: Зависимость остаточного содержания железа(+2) в нефильтрованной воде от исходной концентрации перекиси водорода (1) и от удельной дозы перекиси водорода (2).
Как показывает зависимость остаточного содержания железа(+2) в нефильтрованной воде от удельной дозы перекиси водорода, теоретическая доза окислителя (0,3 мг/мг) обеспечивает окисление не более 20% закисного железа в исходной воде. По-видимому, это может быть объяснено протеканием в реакционном объеме наряду с окислением двухвалентного железа процессов каталитического разложения Н2O2. Для данных условий проведения реакции (без последующего фильтрования) для достижения остаточной концентрации железа(+2) 0,2 мг/дм3 необходим 3-кратный избыток окислителя.
На втором этапе работы исходная вода после обработки перекисью водорода сразу же подвергалась фильтрованию через лабораторный песчаный фильтр (Н = 1,2 м, dф. = 0,8 ÷1,6 мм). В отсутствие Н2O2 фильтрование исходной воды через тот же песчаный фильтр не приводит к заметному снижению содержания в воде ионов железа.
На рис. 2 представлена зависимость остаточного содержания общего железа в фильтрованной воде от исходной концентрации перекиси водорода и удельной дозы окислителя.
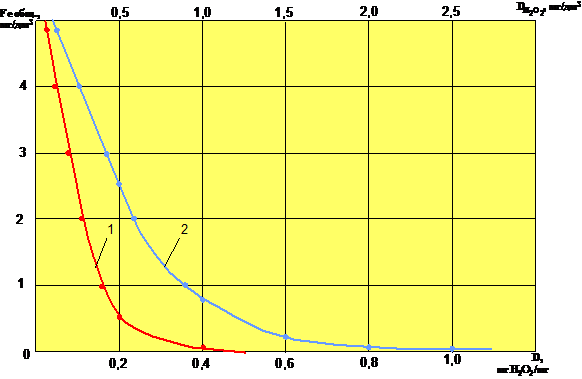
Рис. 2: Зависимость остаточного содержания общего железа в
фильтрованной воде от исходной концентрации перекиси водорода (1)
и от удельной дозы перекиси водорода (2).
Как видно из приведенных данных, применение перекиси водорода в качестве окислителя позволяет практически полностью очистить воду от соединений железа: может быть достигнута его остаточная концентрация менее 0,1 мг/дм3.
Соответствующая зависимость остаточного содержания общего железа в фильтрованной воде от удельной дозы перекиси водорода показывает, что при протекании основной части процесса в фильтрующем слое реакция окисления железа(+2) преобладает. Для получения остаточной концентрации общего железа на уровне 0,05 ÷ 0,10 мг/дм3 избыток окислителя не превышает 30% от стехиометрической (расчетной) дозы.
Полученные в лабораторных условиях результаты проверены на пилотной установке производительностью 2,5 м3/час. Конструкция установки предусматривала возможность обработки как исходной (холодной) воды, подаваемой из распределительной камеры водогрейных резервуаров, так и подогретой воды, подаваемой из распределительного трубопровода фильтровальной станции ВОС г. Новый Уренгой.
Доза окислителя назначалась нами недостаточной для полного окисления закисного железа, остаточная концентрация железа(+2) находилась в пределах 0,1 ÷ 0,2 мг/дм3.
Содержание железа в воде до обработки и после фильтрования приведено в табл.1. Следует отметить, что при обработке холодной воды потребовалось увеличение дозы перекиси водорода в среднем на 11,5 %.
Таблица 1.
|
Тип воды |
Содержание железа, мг/дм3 |
|||
|
исходное |
после обработки |
|||
|
Feобщ. |
Fe(+2) |
Feобщ. |
Fe(+2) |
|
|
Холодная (+10С) |
6,7 ÷6,9 |
5,3 ÷5,4 |
0,1 ÷0,3 |
отс. |
|
Подогретая (+60) |
5,8 ÷6,1 |
4,6 ÷4,7 |
0,1 ÷0,3 |
отс. |
Как видим, температура процесса не влияет на концентрацию железа в фильтрованной воде. Это позволяет отказаться от подогрева перед обработкой подземных вод, что часто применяется на сооружениях водоснабжения в условиях Тюменского севера.
Необходимо отметить также заметное улучшение органолептических показателей качества воды (с 2 до 1 балла).
Полученные результаты использованы при выполнении рабочего проекта «Расширение ВОС г. Новый Уренгой до производительности 65,0 тыс. м3/сут.». Реконструкция станции закончена и в декабре 2007 г. она принята в постоянную эксплуатацию. Содержание железа в очищенной воде не превышает 0,05 мг/дм3. На основании опыта пуско-наладочных работ и пробной эксплуатации разработаны рекомендации по применению этой технологии , позволяющие проектировать станции очистки воды неограниченной производительности.
Купить 50% перекись в Мосрентгене можно, предварительно сделав заказ у нас на сайте.




